Hambasäsi – mida see endas peidab?

Veidi ajalugu
Tüvirakkude ajalugu ulatub tagasi eelmise sajandi keskpaika. Esimese luuüdist pärit tüvirakkude siirdamise tegi 1958. aastal prantsuse onkoloog Georges Mathé. Sel ajal oli tüvirakkude saamiseks ainus võimalus võtta need luuüdist, mis tähendas patsiendi jaoks operatsiooni. Luuüdist saadavaid tüvirakke kasutatakse jätkuvalt ka tänapäeval, kuid lisaks on tüvirakuteaduse arenedes tekkinud uusi võimalusi rakkude saamiseks. Need on palju lihtsamad, mitteinvasiivsed meetodid.
Uued meetodid.
Rohkem kui 35 aastat tagasi hakati tüvirakke hankima nabaväädist ning alates selle sajandi algusest ka hambasäsist. Mõlemal juhul on protseduur lihtne – ei põhjusta valu ega ebamugavust.
Hambasäsi tüvirakkudest teatakse vähem, mistõttu lähemalt just sellest.
Hambasäsi tüvirakud on multipotentsed – võimelised arenema ja diferentseeruma (eristuma) erinevate kudede rakkudeks, neil on immunomoduleeriv funktsioon ja eneseuuendusvõime. Nad on võimelised arenema adipotsüütideks (rasvarakud), närvirakkudeks, odontoblastideks (rakud, millest moodustuvad hamba erinevad struktuurelemendid) ja mitmesugusteks muudeks rakkudeks.
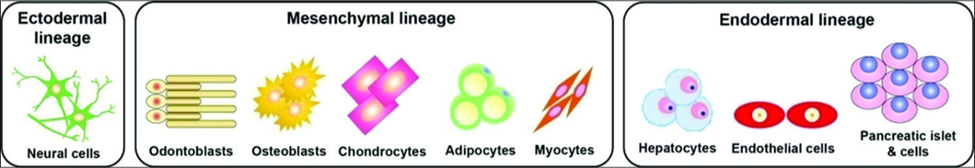
Tüvirakutehnoloogia võimaldab inimese hambasäsi tüvirakkudest (HDPSC – human dental pulp stem cell) saada rakke, mille embrüonaalne päritolu on erinev. Nimelt loote arengu käigus arenevad organismi erinevad rakud erinevatest lootelehe kihtidest (Joonis 1):
- Ektoderm – lootelehe välimine kiht – sellest arenevad närvirakud (1,3)
- Mesoderm – lootelehe keskmine kiht – sellest arenevad odontoblastid, millest moodustuvad hambakoed; osteoblastid, millest moodustuvad luurakud; kondrotsüüdid ehk kõhrerakud, adipotsüüdid ehk rasvarakud ja müotsüüdid ehk südamelihase rakud (4)
- Endoderm – lootelehe sisemine kiht – sellest arenevad vaskulaarsed endoteelirakud ehk veresooneseina rakud (4) hepatotsüüdid ehk maksarakud (5) ja pankrease saarekese insuliini tootvad β-rakud (6)
Joonis 1. Inimese hambasäsi rakkude diferentseerumispotensiaal.
Kas hambasäsi tüvirakud võivad olla paremad kui luuüdist pärit rakud?
Nii luuüdi kui hambasäsi sisaldavad mesenhümaalseid tüvirakke. Mõlemad on väärtuslikud tüvirakkude allikad. Mis on aga erinevus?
Teadaolevalt on hambasäsi tüvirakkudel suurem regeneratiivne potentsiaal kui luuüdist pärinevatel tüvirakkudel. Testides on hambasäsi tüvirakud näidanud 3-4 korda kiiremat paljunemisvõimet (2).
Hambasäsi tüvirakud (DPSC-dental pulp stem cells) avastati esmakordselt 2000. aastal Gronthose ja tema meeskonna poolt (1). DPSC-sid peetakse kraniaalseteks (ajutüvest pärinevad) närvirakkudeks (CNCC), millel on oluline roll embrüo arengus. Hambasäsi tüvirakke (DPSC) peetakse närviharja rakkudeks – see võib omada olulist tähtsust teatud haiguste ravis (2).
Inimese hambasäsist pärinevatel tüvirakkudel on regeneratiivses meditsiinis palju erinevaid võimalusi.
Need on tõhusad mitmesuguste haiguste ja traumade korral. Näiteks võib tuua seljaaju vigastused, Parkinsoni tõbi, Alzheimeri tõbi, ajuisheemia, müokardiinfarkt, lihasdüstroofia, diabeet, maksahaigused, silmahaigused, immuunhaigused suuõõne haigused jm.
Viited
- Gronthos S, Mankani M, Brahim J, Robey PG, Shi S. Postnatal human dental pulp stem cells (DPSCs) in vitro and in vivo. Proc Natl Acad Sci U S A. 2000;97:13625-30.
- Saravana Priyan GL, Subachanya Ramalingam, Yogeshwari Udhayakumar. Human dental pulp stem cells and its applications in regenerative medicine – A literature review. Published: 2019-09-25
- Miura M, Gronthos S, Zhao M, Lu B, Fisher LW, Robey PG, et al. SHED: Stem cells from human exfoliated deciduous teeth. Proc Natl Acad Sci U S A. 2003;100:5807-12.
- Makino Y, Yamaza H, Akiyama K, Ma L, Hoshino Y, Nonaka K, et al. Immune therapeutic potential of stem cells from human supernumerary teeth. J Dent Res. 2013;92:609-15.
- Sonoyama W, Liu Y, Fang D, Yamaza T, Seo BM, Zhang C, et al. Mesenchymal stem cell-mediated functional tooth regeneration in swine. PLoS One. 2006;1:e79.
- Ma L, Aijima R, Hoshino Y, Yamaza H, Tomoda E, Tanaka Y, et al. Transplantation of mesenchymal stem cells ameliorates secondary osteoporosis through interleukin-17-impaired functions of recipient bone marrow mesenchymal stem cells in MRL/lpr mice. Stem Cell Res Ther. 2015;6:104.
